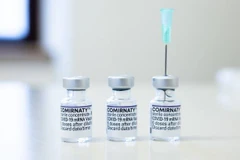
Vắcxin phòng COVID-19 do hãng dược phẩm AstraZeneca phối hợp với Đại học Oxford của Anh bào chế. (Ảnh: AFP/TTXVN)
Vắcxin phòng COVID-19 do hãng dược phẩm AstraZeneca phối hợp với Đại học Oxford của Anh bào chế. (Ảnh: AFP/TTXVN)Cơ quan Quản lý dược phẩm châu Âu (EMA) ngày 12/1 thông báo đã nhận được đơn xin cấp phép có điều kiện loại vắcxin ngừa COVID-19 do hãng dược AstraZeneca và Đại học Oxford nghiên cứu phát triển.
EMA cho biết sẽ xem xét đơn của AstraZeneca trong thời gian ngắn.
Trong thông cáo của mình, EMA cho biết có thể ra quyết định về việc cấp giấy phép cho AstraZeneca vào ngày 29/1, trong cuộc họp của Ủy ban Các sản phẩm thuốc sử dụng cho người (CHMP) thuộc EMA.
[Anh trở thành nước đầu tiên tiêm vắcxin của AstraZeneca/Đại học Oxford]
Trong quá trình xem xét hồ sơ vắcxin của AstraZeneca, EMA đã đánh giá dữ liệu từ các thử nghiệm vắcxin đang được tiến hành tại Anh, Brazil và Nam Phi.
AstraZeneca cũng đã cung cấp thông tin bổ sung theo yêu cầu của CHMP và hiện đang được cơ quan này nghiên cứu.
Cùng ngày, một thành viên của Liên minh châu Âu (EU) là Thụy Điển cho biết đã tiêm vắcxin ngừa COVID-19 cho khoảng 80.000 người kể từ khi bắt đầu triển khai chương trình tiêm chủng vào tháng 12/2020.
Theo dữ liệu của Cơ quan Y tế Công cộng Thụy Điển, tính đến ngày 10/1, nước này đã nhận được khoảng 160.000 liều vắcxin Pfizer/ BioNTech và đã sử dụng khoảng một nửa trong số này.
Cơ quan Y tế Công cộng Thụy Điển cho biết chưa có bất cứ khu vực nào báo cáo gặp sự cố trong quá trình tiêm chủng. Tuy nhiên, một số khu vực đã tiết kiệm vắcxin để có thể tiêm liều thứ 2 bất chấp khuyến nghị của cơ quan này, trong bối cảnh đợt phân phối vắcxin tiếp theo dự kiến sẽ diễn ra theo đúng kế hoạch.
Với dân số khoảng 10 triệu người, Thụy Điển đã tiến hành đợt tiêm chủng đầu tiên từ ngày 27/12 cho nhóm đối tượng là người già trong các viện dưỡng lão, nhân viên các cơ sở này và người thân của họ.
Đợt tiêm chủng thứ hai dự kiến sẽ diễn ra vào tháng 2/2021, dành cho nhóm đối tượng gồm các nhân viên y tế và những người từ 70 tuổi trở lên./.