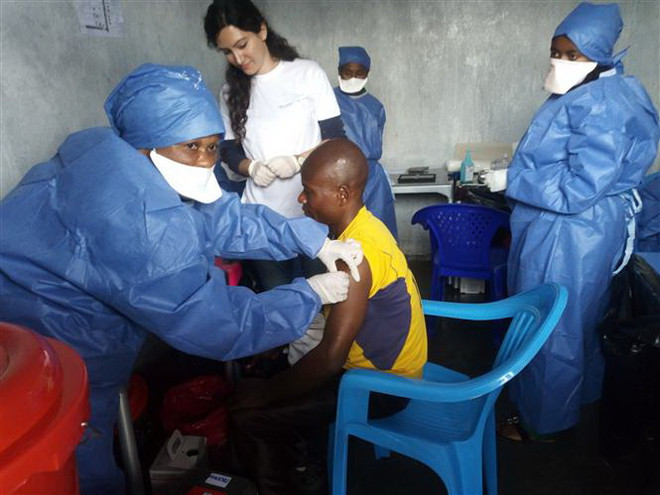
 Tiêm chủng vắcxin phòng Ebola tại Goma, Cộng hòa Dân chủ Congo. (Ảnh: AFP/TTXVN)
Tiêm chủng vắcxin phòng Ebola tại Goma, Cộng hòa Dân chủ Congo. (Ảnh: AFP/TTXVN)Ngày 14/10, Cơ quan Quản lý thực phẩm và dược phẩm (FDA) của Mỹ đã phê duyệt thuốc điều trị Ebola bằng kháng thể tạo ra trong phòng thí nghiệm.
Thuốc có tên gọi là Inmazeb, là một sản phẩm của công ty công nghệ sinh học Regeneron, được FDA phê duyệt sau khi kết quả thử nghiệm lâm sàng cho thấy thuốc giúp giảm đáng kể tỷ lệ tử vong.
Inmazeb được phát triển dựa trên cùng nền tảng công nghệ đã được dùng trong phát triển liệu pháp điều trị bệnh viêm đường hô hấp cấp COVID-19 đang được thử nghiệm của Regeneron. Liệu pháp này đã được đưa vào phác đồ điều trị cho Tổng thống Mỹ Donald Trump sau khi ông nhiễm virus SARS-CoV-2.
Inmazeb là hỗn hợp gồm ba loại kháng thể đơn dòng chống virus hiệu quả cao. Sau khi được tiêm vào tĩnh mạch, Inmazeb kết dính với protein màng (có tên gọi là glycoprotein) của virus Ebola để ngăn chặn protein này xâm nhập vào tế bào cơ thể.
[WHO cảnh báo khả năng lây lan dịch bệnh Ebola ở CHDC Congo]
Thuốc được đưa vào thử nghiệm tại Cộng hòa Congo hồi năm 2018, với 382 bệnh nhân (cả người lớn và trẻ em), chia làm hai nhóm gồm nhóm sử dụng thuốc Inmaze và nhóm còn lại dùng một loại thuốc khác để đối chứng. Kết quả cho thấy tỷ lệ tử vong ở nhóm dùng Inmaze là 33,8% sau 28 ngày, trong khi tỷ lệ tử vong ở nhóm còn lại lên tới 51%.
FDA cho biết tác dụng phụ phổ biến nhất khi dùng Inmaze là sốt, ớn lạnh, tim đập nhanh và thở gấp, song đây là những triệu chứng chung của những người nhiễm virus Ebola. Cơ quan này cũng cảnh báo người đang điều trị bằng Inmaze không nên tiêm vắcxin phòng Ebola bởi tác dụng của thuốc sẽ làm suy yếu hiệu quả của vắcxin.
Tháng 12/2019, FDA cũng đã phê duyệt loại vắcxin đầu tiên phòng virus Ebola có tên gọi Ervebo. Các kháng thể đơn dòng là một loại thuốc tương đối mới được biết đến nhiều trong việc điều trị một số loại bệnh ung thư và bệnh về tự miễn dịch./.